20/07/2022
Strategie diagnostyczne chorób alergicznych
Niezwykle zróżnicowane fenotypy alergii o powodują, że z koniecznością rozpoznawania alergicznego patomechanizmu objawów klinicznych mierzyć się muszą lekarze różnych specjalności. I tak, objawami dermatologicznymi alergii, niezależnie od drogi ekspozycji na alergen, mogą być: wysypka, pokrzywka, wyprysk atopowy, obrzęk naczyń czy suchość skóry. Objawami z układu oddechowego: astma, nieżyt nosa, obrzęk krtani, zapalenie uszu, nawracające zakażenia górnych dróg oddechowych, którym towarzyszyć może podrażnienie spojówek, łzawienie oczu etc. Symptomami ze strony przewodu pokarmowego: bóle brzucha, nudności, wymioty, biegunka, wzdęcia, brak apetytu. Obserwowane są niekiedy objawy neurologiczne lub dolegliwości psychiczne: bóle głowy, zaburzenia snu, nadmierna ruchliwość, rozdrażnienie, stany depresyjne i objawy psychotyczne (reaktywne zaburzenia psychiczne).
Wczesne wdrożenie leczenia alergii, z naciskiem na przyczynową terapię swoistą, wymagające dokładnej identyfikacji czynnika uczulającego, jest podstawą sukcesu terapeutycznego. W klasycznym algorytmie diagnostycznym, typowanie alergenu uczulającego oraz rozpoznanie prawdopodobnego mechanizmu immunologicznego reakcji uczuleniowej, były weryfikowane przez identyfikację alergenowo swoistych przeciwciał IgE in vivo (dodatnia reakcja w testach skórnych, SPT) i in vitro (pomiar stężenia) lub przez określanie miejscowej reakcji komórkowej zależnej od przeciwciał IgE (reakcja eozynofilowa, aktywacja bazofili etc.). Powszechna, zwłaszcza w przypadku SPT, akceptacja testów diagnostycznych identyfikujących sIgE, powodowała, że niekiedy pomijano ich istotne ograniczenie polegające na rozpoznawaniu wyłącznie uczulenia na alergen (ang. sensitization), które nie musi być równoznaczne z alergią objawiającą się klinicznie.
Metody laboratoryjne stosowane w pomiarach stężenia sIgE w próbkach krwi in vitro
Testy stosowane w laboratoryjnej diagnostyce alergii opartej na pomiarach stężenia alergenowo-swoistej IgE in vitro różnią się szczegółami metodycznymi i rozwiązaniami technicznymi (tzw. formatami) oraz liczbą równocześnie analizowanych alergenów (monopleksy, multipleksy etc). Jednakże bez względu na szczegóły techniczne wszystkie hołdują zasadom analizy instrumentalnej i podlegają standaryzacji opartej na międzynarodowych wzorcach IgE (np. 3rd WHO International Standard of IgE). Ich precyzja i dokładność jest dużo lepsza niż testów skórnych (Tabela poniżej). Wyniki testów pochodzących od różnych producentów są porównywalne, a rozłożone w czasie monitorowanie postępów choroby lub efektów terapii staje się miarodajne. Należy jednak pamiętać, że tak jak w przypadku innych badań laboratoryjnych, długotrwały monitoring pacjenta lub rozszerzanie zakresu diagnostyki, powinny być oparte na jednej metodzie i formacie testu lub systemach testowych tego samego producenta.
W testach skórnych nieswoiste podrażnienia obserwowane są w 50-60% badanych. Czy to wystarczy by ogłosić koniec supremacji testów skórnych?! (wg Scientific American 2015, artykuł redakcyjny).
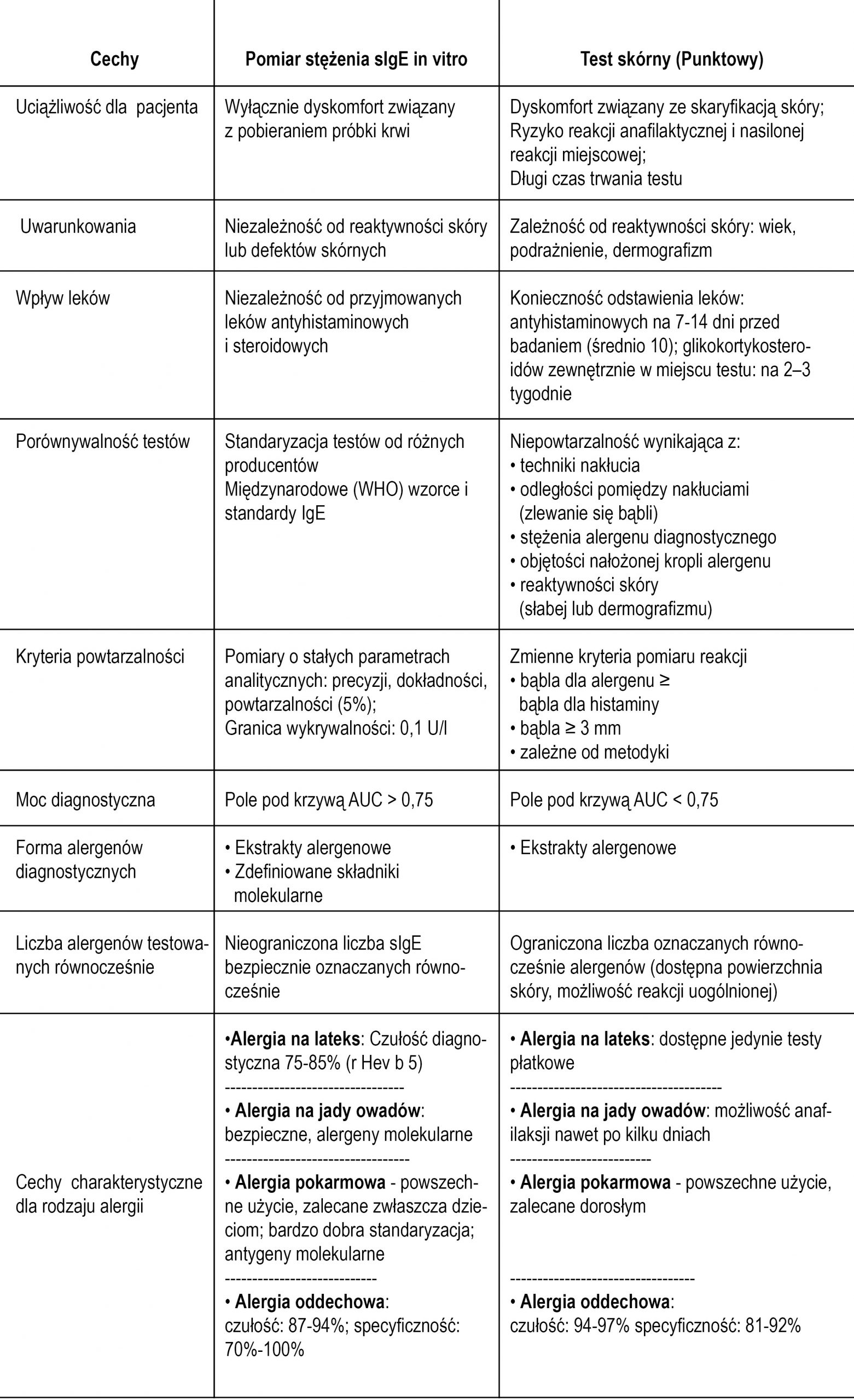
Zestawienie wad i zalet pomiarów sIgE we krwi obwodowej i testów skórnych (SPT) w diagnostyce alergii
Zestawienie właściwości obu testów – skórnego i in vitro, wskazuje na konieczność weryfikacji, słabnącego na szczęście, przekonania o bezwarunkowej wyższości testów skórnych nad pomiarami sIgE in vitro. W zestawieniu uwzględniono: zagrożenia i uciążliwości dla badanego, zależność wyniku od cech osobniczych i przyjmowanych leków, standaryzację metod, parametry analityczne i moc diagnostyczną oraz przydatność z zależności typu diagnozowanej alergii.
Laboratoryjna diagnostyka alergii – atuty pomiarów sIgE in vitro
W dziedzinie diagnostyki laboratoryjnej in vitro poczyniono znaczne, niekiedy nawet rewolucyjne postępy, choć wydaje się, że rozwój laboratoryjnych technik diagnostycznych był, a niekiedy jeszcze jest, mocno niedoceniony przez lekarzy alergologów. W porównaniu, choćby do początku obecnego stulecia, dalece udoskonalono metody pomiaru sIgE i produkcję alergenów diagnostycznych w oparciu o techniki inżynierii genetycznej, uzyskując poprawę parametrów analitycznych (np. granicy wykrywalności z 0,35 kU/l do 0,1 kU/l) i diagnostycznych: czułości, specyficzności i dodatniej wartości predykcyjnej (PPV). Równocześnie wzbogacono testy o nieosiągalne dotąd możliwości prognostyczne, dotyczące: prawdopodobieństwa manifestacji klinicznej, nasilenia i charakteru reakcji alergicznych (miejscowa/uogólniona/anafilaktyczna), zagrożenia i ryzyka skutków fatalnych, możliwości rozwoju (marsz alergiczny) i optymalizacji profilaktyki i leczenia. Bardzo bliski wdrożenia do rutynowej diagnostyki laboratoryjnej jest test BAT (ang. basophil activation test), odzwierciedlający in vitro początkową fazę zależnej od IgE odpowiedzi natychmiastowej, na etapie, gdy poziom IgE jest jeszcze zbyt niski dla oznaczeń we krwi obwodowej, a także umożliwiający określanie poziomu tolerancji alergenu. Zastosowanie BAT w klinice alergii przyniesie korzyści w rozpoznawaniu stanów alergicznych zależnych od IgE, monitorowaniu rozpoznanej alergii oraz ocenie odpowiedzi na leczenie immunomodulujące.
Pomiar sIgE we krwi obwodowej jest powszechnie dostępną, nieuciążliwą i bezpieczną dla pacjenta, laboratoryjną metodą diagnostyki chorób alergicznych, komplementarną do ambulatoryjnej identyfikacji sIgE in vivo w punktowych testach skórnych, SPT (ang. skin prick test). W odróżnieniu od testów skórnych, identyfikacja i pomiary sIgE in vitro nie wymagają przygotowania badanego do badania, w tym, przede wszystkim, odstawienia leków przeciwhistaminowych i steroidowych stosowanych miejscowo i systemowo.
Jako badanie z wyboru, pomiar stężenia sIgE in vitro zlecany jest u małych dzieci, osób w trakcie leczenia lekami przeciwhistaminowymi lub steroidowymi, osób z defektami i chorobami skóry oraz w przypadku obaw wystąpienia reakcji anafilaktycznej w następstwie testu skórnego.
Niedostępna dla SPT precyzja i standaryzacja pomiarów sIgE in vitro pozwala na wyznaczanie zależności pomiędzy stężeniem IgE specyficznej dla określonego alergenu, prawdopodobieństwem uczulenia na ten alergen i ekspresji objawów klinicznych uczulenia. Uzyskany w ostatnich latach trzykrotny wzrost czułości analitycznej pomiaru sIgE in vitro powoduje, że prócz waloru diagnostycznego, wielkość stężenia sIgE posiadła walor prognostyczny. W piśmiennictwie i materiałach walidacyjnych testów określających stężenie sIgE w krwi obwodowej, moc diagnostyczna pomiaru, wyrażana przez powszechnie przyjęte parametry: powierzchnię pola pod krzywą ROC (ang. Receiver Operating Characteristic), opisywanego skrótem AUC (ang. Area Under the (ROC) Curve) oraz iloraz szans, OR (ang. odds ratio), jest większa niż moc diagnostyczna testów skórnych pośrednio odzwierciedlających miejscowy poziom sIgE i do tego w miejscu odległym od regionu dotkniętego objawami alergii.
Atutem pomiarów stężenia sIgE in vitro jest:
- Bezpieczeństwo i mała uciążliwość dla badanego (badanie z wyboru u małych dzieci) – krótkotrwały dyskomfort związany z pobieraniem próbki krwi;
- Dostępność badania – możliwość pobrania próbki krwi w punktach pobrań materiału do rutynowych laboratoryjnych badań diagnostycznych;
- Niezależność wyniku badania od stosowanych aktualnie leków antyhistaminowych i przeciwzapalnych – możliwość wykonywania badania bez przerywania terapii;
- Niezależność wyniku badania od krótkotrwałych zmian skórnych lub trwałych defektów skórnych (dermografizm) ograniczających stosowanie testów skórnych;
- Możliwość równoczesnej identyfikacji praktycznie nieograniczonej liczby sIgE;
- Doskonała standaryzacja metody pomiarowej i stosowanych alergenów diagnostycznych;
- Możliwość oparcia pomiarów sIgE na zdefiniowanych i modyfikowanych preparatach alergenowych wytwarzanych przy użyciu biotechnologii i inżynierii genetycznej;
- Walor prognostyczny obok zastosowania diagnostycznego.
Dr Tomasz Ochałek,
Laboratoria Medyczne DIAGNOSTYKA
Wybrana pozycja piśmiennictwa
- Goswami K : Qualitative Assessment of Allergen Skin Test and In vitro Allergen Specific Immunoglobulin E (IgE) Measurement as a Method of Detection of Allergic Symptoms. Int.J. Curr. Microbiol. App. Sci. 2016, 5 : 614-619.
- O. et al: Basophil Activation Test: Old and New Applications in Allergy. Curr Allergy Asthma 77, 2018.
- Roberts G, Lack G. Diagnosing peanut allergy with skin prick and specific IgE testing. J Allergy Clin Immunol. 115, 1291–1296, 2005.
Zachęcamy do przeczytania pozostałych artykułów o Alergiach, przygotowanych przez naszych specjalistów:
ALERGIA I – Od ekstraktów do alergenów molekularnych
ALERGIA III -Diagnostyka molekularna alergii
ALERGIA IV – Implikacje kliniczne i diagnostyczne pomiarów sIgE
