12/03/2016
Najistotniejsze laboratoryjne badania diagnostyczne wątroby dzielą się na:
- Badania krwi diagnozujące cholestazę: ALP (fosfataza zasadowa), GGT (gamma-glutamylotranspeptydaza), bilirubina. Substancje te powstają w drogach żółciowych i ich stężenie w krwi wzrasta w przypadku zapalenia lub zablokowania dróg żółciowych (w wątrobie, poza wątrobą lub w obu lokalizacjach).
- Badania krwi diagnozujące uszkodzenie komórek wątrobowych: ALT (aminotransferaza alaninowa), AST (aminotransferaza asparaginianowa)
- Badania krwi oceniające ogólnie funkcje wątroby: spadek stężenia albuminy, wzrost INR (znormalizowany czas protrombinowy), wzrost bilirubiny, spadek glukozy. Patologiczne wyniki tych oznaczeń świadczą o poważnym uszkodzeniu dużej części komórek wątrobowych, jednakże mogą być spowodowane szeregiem innych stanów patologicznych.
Ogólnie:
- ALT/AST – markery wątrobokomórkowe (enzymy indykatorowe) wzrastają w efekcie:
wirusowego zapalenia wątroby, alkoholizmu, przyjmowanych leków i preparatów ziołowych, hemochromatozy, autoimmunizacyjnych chorób wątroby. - ALP/GGT/bilirubina – markery cholestazy wzrastają w efekcie:
kamicy żółciowej, oporów patologicznych w jamie brzusznej (masy brzusznej), przyjmowanych leków, ciąży, pierwotnej marskości
wątroby, paraneoplazji (zwłaszcza w przypadku chłoniaka), posocznicy.
Żaden z wymienionych enzymów indykatorowych nie jest ściśle specyficzny dla wątroby. Przykładowo: ALP wzrasta także w przypadku chorób kości, deficytu witaminy D, w III trymestrze ciąży (pozostałe enzymy pozostają w normie); AST w chorobach mięśni szkieletowych.
Inne laboratoryjne oznaczenia stosowane w diagnostyce wątroby:
- LDH – w przebiegu chorób wątroby, zwłaszcza zapalenia wątroby, obserwowany jest wzrost dehydrogenazy mleczanowej (LDH), jednakże jego swoistość diagnostyczna jest niewielka.
- ChE – cholinoesteraza enzym estrolityczny syntetyzowany w wątrobie i wydzielany do krwi (występuje w trzustce i innych tkankach organizmu). Oznaczenie aktywności cholinoesterazy w surowicy jest wskaźnikiem funkcji wątroby. Zmniejszenie aktywności (stężenia) enzymu jest sygnałem uszkodzenia miąższu wątroby. Towarzyszy marskości i nagminnemu zapaleniu wątroby. Obserwowane jest również w chorobach nowotworowych, zakaźnych i ostrych stanach zapalnych, zatorach płucnych, zawale mięśnia sercowego i dystrofii mięśniowej.
- AFP (alfafetoproteina) – podniesione stężenie AFP we krwi obserwowane jest u osób chorych na ostre wirusowe zapalenie wątroby typu B i C, przewlekłe aktywne zapalenie wątroby, marskość wątroby i alkoholową marskość wątroby. Wzrost AFP obserwowany jest również w przypadku raka wątrobowokomórkowego, lecz oznaczenie to nie ma waloru badania przesiewowego.
Laboratoryjne badania wątroby zlecane są najczęściej:
- w przypadku złego samopoczucia pacjenta, znużenia (u osób ponad 50 letnich dłuższego niż miesiąc), świądu, ból brzucha
(prawy górny kwadrant), gorączki nieznanego pochodzenia itd. - w przypadku dodatnich testów serologicznych w kierunku HBV i HCV
- w przypadku istnienia czynników ryzyka stłuszczenia wątroby: otyłości brzusznej, podejrzenia cukrzycy, silnie patologicznego lipidogramu
- rutynowo: u osób przyjmujących określone leki i w ostrej reakcji polekowej
- sporadycznie: w przypadku złego samopoczucia u osób przyjmujących leki
- przy podniesionym stężeniu ferrytyny i żelaza oraz w hemochromatozie
- w przypadku chorób o tle autoimmunizacyjnym i przerzutów nowotworowych
- w przypadku zapalnych chorób jelit
- w przypadku chorób wątroby i/lub nieprawidłowych wyników testów wątrobowych w przeszłości
- w przypadku podejrzenia ostrego zatrucia alkoholem
- w przypadku nieprawidłowych wyników ogólnych badań laboratoryjnych: nieprawidłowej morfologii (wysokie MCV, neutropenia, trombocytopenia), niedoboru alfa1-antytrypsyny itd.
- w przypadku podejrzenia żółtaczki i ostrego zapalenia wątroby.
Zapalenie wątroby
Zapalenie wątroby (hepatitis) poza obrazem histologicznym wiążę się z podniesionymi ALT i AST. Stężenie ALT i AST > 500 U/l, a zwłaszcza
> 1000U/l, przy ALP i GGT < 300 U/l świadczy o zakażeniu wirusowym. W chronicznym zapaleniu wątroby zmiany ALT odzwierciedlają aktywność choroby. W przypadku zapalenia wątroby typu C poziom enzymów wątrobowych jest prawidłowy lub nieznacznie przekracza zakres, lecz wzrasta pod wpływem substancji hepatotoksycznych.
(wg.Sonic Pathology Handbook. A quide to the interpretation of pathology tests. Ed. Campbell Kyle. Sonic Healthcare Ltd. 2014).
Do głównych przyczyn zapalenia wątroby należą:
1. zakażenia wirusami:
- HAV – wirusowe zapalenie wątroby typu A (WZW A)
- HBV – wirusowe zapalenie wątroby typu B (WZW B)
- HCV – wirusowe zapalenie wątroby typu C (WZW C)
- EBV – mononukleoza zakaźna
- HDV, HEV – wirusowe zapalenie wątroby D, E
- HIV, CMV, Coxsackie, wirusy dające objawy grypopodobne
2. leki
3. alkohol
4. choroby autoimmunizacyjne
5. hepatotoksyny (czterochlorek węgla), egzotyczne zioła lecznicze
WIRUSOWE ZAPALENIE WĄTROBY typu: A, B, C
SEROLOGICZNE I MOLEKULARNE BADANIA W WIRUSOWYM ZAPALENIU WĄTROBY TYPU B (WZW B)
Markery wirusa zapalenia wątroby typu B – HBV:
HBsAg, anty-HBc IgM, anty-HBc total (IgM, IgG), anty-HBs, HBeAg, anty-HBeAg, HBV DNA (PCR)
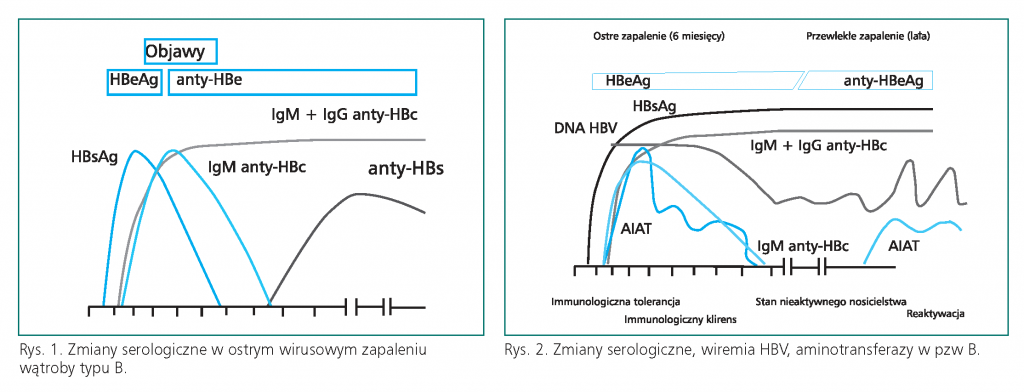
HBs antygen (HBsAg) – Antygen powierzchniowy (s: ang. surface) występujący we krwi osoby zakażonej. Jest pierwszym markerem zakażenia HVB, a jego obecność we krwi często wyprzedza objawy zakażenia. HBsAg można wykryć już 4 tygodnie od zakażenia (średnio 4-12 tygodni). Zanikanie HBsAg – zwykle od 2 do 4 miesięcy od pojawienia się objawów – jest oznaką zdrowienia po ostrym zapaleniu. Utrzymywanie się HBsAg we krwi przez ponad 6 miesięcy jest klasyfikowane jako nosicielstwo wirusa.
HBe antygen (HBe Ag) – Antygen wczesny (e: ang. early) utrzymuje się we krwi do 10 tygodni (pojawia się średnio od 3-6 tygodni po zakażeniu). Jest markerem intensywnej replikacji wirusa, a jego obecność wskazuje na ostre, aktywne, zakażenie i wysoką zakaźność. Oznaczenie HBe Ag może również służyć do monitorowania skuteczności leczenia zakażenia wirusem B. Istnieją rzadkie w Polsce typy wirusa HBV, które nie produkują antygenu HBe. Utrzymywanie się HBe Ag we krwi dłużej niż 10-12 tygodni może wskazywać na przejście zakażenia w stan przewlekły.
HBc przeciwciała (anty-HBc) – Są wytwarzane przez organizm w okresie ostrego zakażenia HBV i po jego przebyciu. Występują prawie równocześnie z antygenem HBs. Przeciwciała w klasie IgM mogą utrzymywać się we krwi nawet do 2 lat – zwykle zanikają po okresie od 3 do 24 miesięcy. Obecność IgM HBc, nawet przy ujemnym wyniku HBsAg, wskazuje na ostre zakażenie HBV. Przeciwciała klasy IgG (anty-HBc IgG) utrzymują się przez lata. Oznaczane są testem HBc Przeciwciała całkowite (total).
HBs przeciwciała (anty-HBs) – Obecność anty-HBs wskazuje na kontakt z antygenem wirusa HBV w przeszłości i świadczy o nabyciu odporności w wyniku szczepienia lub przebytego WZW B. Unieszkodliwiają one wirusa, chroniąc przed zakażeniem. Pojawiają się po ustąpieniu objawów chorobowych i po zaniknięciu antygenu HBs (HBsAg), średnio w okresie 3-4 miesięcy. Mogą występować we krwi do 6 lat po zakażeniu.
HBe przeciwciała (anty-HBe) – Pojawiają się po zaniknięciu antygenu HBe (średnio 4-5 miesięcy po zakażeniu). Obecność przeciwciała anty-HBe wraz z eliminacją HBeAg wskazuje na zdrowieniu po ostrym zakażeniu HBV.
Metody PCR – Reakcja łańcuchowa polimerazy, PCR (ang. polymerase chain reaction) badanie materiału genetycznego HBV (DNA), wykonywany jest w powiązaniu z rutynowymi testami serologicznymi (wykrywaniem antygenów i przeciwciał). Jakościowa PCR wykrywa obecność DNA wirusa w krwi i ma znaczenie diagnostyczne, podczas gdy ilościowa PCR określa liczbę kopii wirusa. Pozwala na określenie wrażliwości HBV na leki, prognozowanie i monitorowanie terapii w oparciu o zmiany liczby kopii wirusa w krwi: spadek w przypadku podatności na leczenie i wzrost związany z powstawaniem mutantów odpornych.
SEROLOGICZNE I MOLEKULARNE BADANIA W WIRUSOWYM ZAPALENIU WĄTROBY TYPU C (WZW C)
Markery wirusa zapalenia wątroby typu C – HCV: anty-HCV, HCV RNA (PCR), genotypy HCV
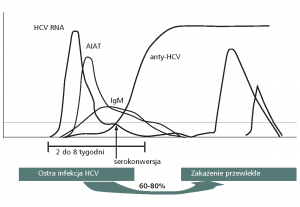
HCV przeciwciała (anty-HCV) – Przeciwciała anty-HCV wykrywane w obecnych testach przesiewowych dla HCV na ogół są immunoglobulinami IgG, swoistymi w stosunku do antygenów kodowanych przez cztery różne regiony genomu wirusa. Wykrywane są najczęściej 8-9 tygodni po zakażeniu, które zwykle przebiega bezobjawowo. Oznaczenie anty-HCV ma charakter jakościowy. Wynik dodatni świadczy o kontakcie z HCV. Nie pozwala natomiast na rozróżnienie zakażenia ostrego od przewlekłego (w około 80 procentach przypadków), zakażenia aktualnego od zakażenia w przeszłości i nie rozstrzyga o eliminacji wirusa.
Przeciwciała anty-HCV. Test potwierdzenia Immunoblot. – Zgodnie z zaleceniami, nisko dodatni lub nieokreślony wynik oznaczenia przeciwciał anty-HCV w teście przesiewowym powinien być potwierdzony. Jedną z zalecanych metod potwierdzenia jest rekombinowany immunoblot (RIBA), wykazujący reaktywność przeciwciał oddzielnie w stosunku do kilku rekombinantowych składników antygenów. Testem RIBA RecomLine oznaczana jest reaktywność IgG w stosunku do antygenów HCV: Core 1,
Core 2, helikazy, NS3, NS4 i NS5. Za prawdziwie dodatni uznaje się wynik, w którym odpowiednio intensywna reakcja barwna zachodzi w przypadku wymaganej liczby antygenów.
Metody PCR – Najbardziej wiarygodnym testem wykazującym zakażenie HCV jest identyfikacja jego materiału genetycznego – RNA. RNA HCV może być wykryty (metodą jakościową lub ilościową) w ciągu 1-2 tygodni po zakażeniu, czyli kilka tygodni przed pojawieniem się anty-HCV i wzrostem poziomu enzymów wątrobowych. Jedną z metod wykrywania RNA wirusa jest reakcja łańcuchowa polimerazy, PCR ( ang. polymerase chain reaction), z odwrotną transkrypcją (RT PCR). Metody ilościowe pozwalają na wykrycie kilkuset kopii RNA wirusa w ml. Oznaczenie ilości RNA HCV jest istotne w określaniu przebiegu zakażenia HCV i odpowiedzi na leczenie. Monitorowanie liczby kopii RNA we wczesnym etapie leczenia informuje o podatności na leczenie. Największe prawdopodobieństwo ustalenia ostrego zakażenia HCV daje wykrycie obecności wirusowego RNA lub antygenu rdzeniowego, przy jednoczesnym braku przeciwciał anty-HCV.
Genotypowanie – Genotypowanie HCV (identyfikacja genotypu) jest przydatne w prognozowaniu długości i intensywności terapii antywirusowej w WZW C. W diagnostyce HCV wyróżnia się 6 podstawowych genotypów HCV, o homologii nukleotydów mniejszej niż 70% oraz liczne podtypy. HCV jako wirus RNA charakteryzuje się wysokim stopniem spontanicznych mutacji, które u przewlekle chorych powodują powstawanie kolejnych quasigatunków wirusa. Chorzy zakażeni wirusem o genotypach 2, 3 i 4 wykazują dwukrotnie wyższy stopień odpowiedzi na leczenie niż zakażeni pozostałymi genotypami. Leczenie zakażenia HCV o genotypach 2 i 3 wykazuje skuteczność po 6 miesiącach, podczas gdy pozostałe genotypy wymagają terapii 12 miesięcznej.
SEROLOGICZNE I MOLEKULARNE BADANIA W WIRUSOWYM ZAPALENIU WĄTROBY TYPU A (WZW A)
Markery wirusa zapalenia wątroby typu A – HAV: anty-HAV IgM, anty-HAV total (IgM+IgG)
HAV przeciwciała IgM (anty-HAV IgM) – Ich obecność stwierdzana jest u > 95% chorych w ostrym okresie choroby: diagnozowanych w kierunku WZW A z powodu objawów i utrzymują się przez 3-6 miesięcy. Przetrwała IgM anty-HAV może występować u osób, które przebyły chorobę w odległej przeszłości lub u dzieci poniżej 5 lat, przechodzących bezobjawowe zakażenie HAV.
HAV przeciwciała całkowite (total anty-HAV, IgM+IgG) – Przeciwciała anty-HAV IgG mogą występować łącznie z IgM w okresie choroby objawowej (do serokonwersji dochodzi nieznacznie później niż w przypadku IgM) i utrzymują się do końca życia. Stwierdzane są u noworodków jako efekt nabytej odporności matczynej i w wyniku szczepienia.
Przeciwciała w autoimmunizacyjnych chorobach wątroby
AUTOIMMUNIZACYJNE ZAPALENIE WĄTROBY AIH (ang. autoimmune hepatitis)
AIH typu 1 (AIH 1) – Markerem klasycznego autoimmunizacyjnego zapalenia wątroby typu 1 AIH (ang. autoimmune hepatitis) są przeciwciała przeciw mięśniom gładkim, ASMA (ang. smooth muscle antibodies). W wysokim stężeniu (mianie) występują u ponad 80% chorych. Stężenie ASMA może korelować z aktywnością choroby, choć niskie stężenia są nieswoiste, gdyż mogą się wiązać z zakażeniami wirusowymi. U kobiet w przypadku pierwotnego AIH 1 stwierdzana jest obecność przeciwciał przeciwjądrowych ANA. W przypadku braku przeciwciał ASMA/ANA w różnicowaniu AIH 1 i AIH 2 przydatne jest oznaczenie przeciwciał przeciw cytoplazmie neutrofili p-ANCA, stwierdzanych wyłącznie u 40-96 % chorych na AIH 1. Przeciwciała przeciw aktynie stwierdzane są u 40-90% chorych. W podobnym odsetku chorych występują przeciwciała przeciw rozpuszczalnemu antygenowi wątroby (SLA) i antygenowi wątrobowo-trzustkowemu (LP).
AIH typu 2 (AIH 2) – Markerami AIH 2 są przeciwciała przeciw mikrosomom wątroby i nerek (LKM-1) oraz przeciw antygenowi cytoplazmatycznemu wątroby (anty-LC-1), występujące u 30% chorych, o mianie dodatnio skorelowanym ze stopniem aktywności choroby. Poza AIH-2, LKM są stwierdzane w przypadku WZW C i w polekowego zapalenia wątroby.
AIH typu 3 (AIH 3) – Typ AIH 3 został wyróżniony na podstawie występowania przeciwciał innych niż w AIH 1 i AIH 2. Charakteryzuje się obecnością przeciwciał SLA i LP. Klinicznie AIH 3 jest identyczne z AIH 1.
PIERWOTNA MARSKOŚĆ ŻÓŁCIOWA PBC (ang. primary biliary cirrhosis).
Swoistym i czułym markerem PBC są przeciwciała przeciwmitochondrialne: AMA i AMA M2 (przeciwciała przeciwmitochondrialne typu M2). Występują u około 95 % chorych.
Przeciwciała przeciwko kanalikom żółciowym BDA, BCA występujące w chorobach wątroby o podłożu autoimmunizacyjnym, stwierdzane są
u 75% chorych na PBC.
PIERWOTNE STWARDNIAJĄCE ZAPALENIE DRÓG ŻÓŁCIOWYCH, PSC (ang. primary sclerosis cholangitis).
Najczęściej wykrywane przeciwciała to ANA, ASMA (ok.20-50% chorych) i p-ANCA (ok. 30-80% chorych).
