28/06/2021
Chociaż zakażenie większością typów HPV ustępuje samoistnie (w 90% przypadków) i przebiega bezobjawowo, to uporczywe zakażenie pewnymi typami doprowadza do stanów patologicznych (np. atypii komórkowej), przeradzających się w zmiany nowotworowe o charakterze złośliwym. HPV o takich właściwościach określane są jako typy wysokiego ryzyka rozwoju nowotworu i zaliczane do wirusów onkogennych. Związek z chorobami nowotworowymi przypisywany jest ok. 100 typom HPV, przy czym większość z nich należy do grup o średnim i niskim ryzyku indukcji nowotworu. Przesłanką o potencjale onkogennym danego typu HPV jest identyfikacja jego DNA w genomie komórek transformowanych nowotworowo. Do HPV wysokiego ryzyka zaliczono 12 typów: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 i 59, typami HPV niskiego ryzyka są: 6, 11, 40, 42, 43, 44, 54, 61 i 72 powodujące choroby łagodne, m.in. brodawczaki narządów płciowych. 13 typów HPV uznano za prawdopodobnie rakotwórcze.
Większość infekcji HPV objawiających się klinicznie wiąże się z HPV-16 i 18 oraz 6 i 11. HPV typu 16 i 18 powodują około 70% przypadków raka szyjki macicy, HPV-6 i 11 są odpowiedzialne za 95-100% brodawek narządów płciowych u kobiet i mężczyzn. Rozwojem nowotworów złośliwych w konsekwencji zakażenia HPV zagrożone są szczególnie osoby z niedoborami odporności, w tym zakażone HIV. U osób immunokompetentnych większość zmian łagodnych wywołanych przez HPV ustępuje zwykle samoistnie. Poza kontaktami seksualnymi wszystkich rodzajów, HPV przenoszą się przez kontakt dotykowy, kontakt ze skażoną odzieżą, ręcznikami etc. i rzadko na drodze okołoporodowej transmisji na dzieci matek z brodawkami narządów płciowych (HPV 6/11). U dziecka może dojść wtedy do tzw. nawracającej brodawczakowatości dróg oddechowych polegającej na rozwoju kilku brodawczaków krtani i tchawicy.
Rocznie, na świecie, HPV powodują ponad 600 000 przypadków nowotworów, w tym: raka szyjki macicy, sromu i pochwy, raka odbytu i odbytnicy, prącia oraz niektórych nowotworów jamy ustnej i gardła (tylnej części gardła, podstawy języka i migdałków).
Obecność DNA HPV zidentyfikowano w 99,7% przypadków wspomnianego na początku raka szyjki macicy, stanowiącego czwarty pod względem częstości nowotwór kobiet, z 569 847 przypadkami nowych zachorowań i ponad 311 000 zgonów (7,5% zgonów kobiet z przyczyn onkologicznych) w 2018 roku. W afrykańskich czy południowoamerykańskich krajach rozwijających się częstość raka szyjki macicy osiąga 40 przypadków na 100 000 kobiet.
HPV należy do wirusów rodziny Papillomaviridae (łac. „papilla” oznacza krosty), wyodrębnionej przez Międzynarodowy Komitet Taksonomii Wirusów, ICTV (ang. International Committee on Taxonomy of Viruses) w 2000 roku. Jest niewielkim (średnica 50-55 nm), bezotoczkowym wirusem z kołowym genomem dwuniciowego DNA o ciężarze 7–8 kbp, odpornym na ciepło, wysuszenie, kwasy i eter. Wszystkie HPV kodują cztery konserwatywne białka rdzeniowe, a HPV onkogenne, dodatkowo, regulatorowe białka: E5, E6 i E7 – odpowiedzialne za onkogenezę. E5 uczestniczy w różnicowaniu keratynocytów, ułatwiając zainfekowanym komórkom unikanie mechanizmów obronnych gospodarza w późniejszych etapach transformacji, natomiast E6 i E7, dwa onkogeny główne, zwane niekiedy w piśmiennictwie anglojęzycznym „oncoplayers” („onkosprawcy”) dezorganizują komórkowe mechanizmy kontrolne, prowadząc do transformacji charakterystycznej dla komórek nowotworowych. E6 i E7 stanowią biomarkery raka szyjki macicy i cele opracowywanych strategii terapeutycznych. Wczesne białka: E1 i E2 reguluje replikację genomu HPV i transkrypcję pozostałych wczesnych białek, E4 reguluje uwalnianie cząsteczek HPV z komórki.
Dotychczas zidentyfikowano ponad 200 typów chorobotwórczych HPV, na podstawie struktury DNA zaszeregowanych do pięciu rodzajów: Alpha-, Beta-, Gamma-, Mu- i Nupapillomavirusów. Większość (z rodzajów: beta i gamma) prowadzi do infekcji subklinicznych lub bezobjawowych, natomiast rodzaj alfa zawiera typy zaliczane do wirusów onkogennych (onkowirusów).
Ewolucja genetyczna HPV jest bardzo powolna. Udało się odtworzyć różnicowanie genetycznych wariantów HPV na przestrzeni ostatnich 200 tys. lat, a znajomość genetycznego dryftu wirusa wykorzystano do monitorowania migracji dawnych populacji ludzkich.
HPV wykazuje wysoki tropizm do komórek warstwowego nabłonka płaskiego, przy czym replikuje wyłącznie w komórkach ulegających proliferacji. Po wniknięciu do komórki wirus może pozostać w stanie utajonym lub ulegać aktywnej replikacji.
Atakujący skórę lub błonę śluzową HPV wykorzystuje skomplikowany proces odnowy wielowarstwowego nabłonka płaskiego.
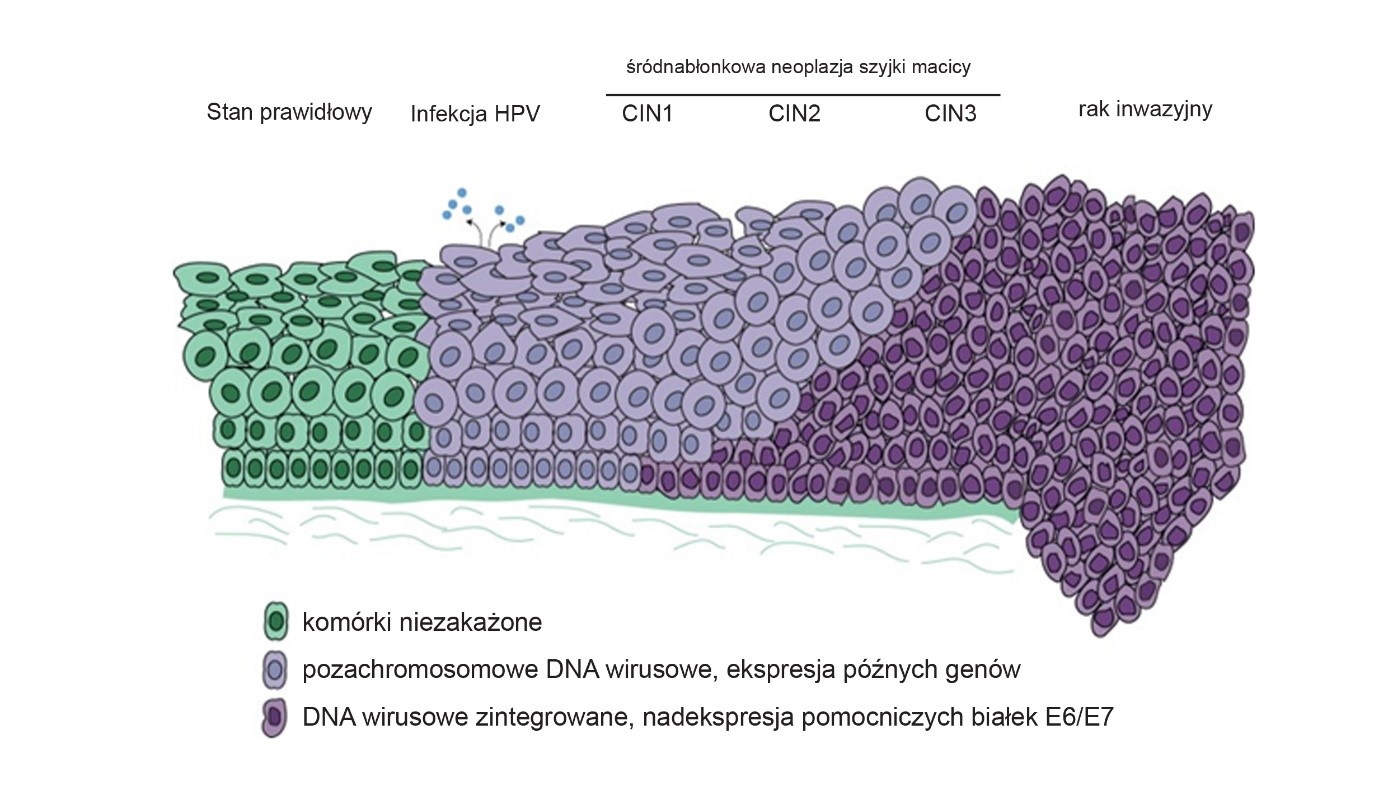
Progresja zmian w kierunku raka szyjki macicy następująca w wyniku zakażenia wirusem HPV typu wysokiego ryzyka. Etapy progresji CIN (ang. cervical intraepithelial neoplasia) – śródnabłonkowej neoplazji szyjki macicy – od zakażenia HPV do inwazyjnego raka szyjki macicy. Klasyfikacja CIN uwzględnia oceną histologiczną badanej tkanki: grubość nabłonka z nieprawidłowymi zmianami, stopień aktywności mitotycznej i atypii komórkowej.
- CIN 1 – neoplazja śródnabłonkowa szyjki macicy małego stopnia (najłagodniejsze zmiany komórek – ang. mild dysplasia). LSIL w systemie Bethesda
- CIN 2 – neoplazja śródnabłonkowa szyjki macicy dużego stopnia (średnie przemiany komórek – ang. moderate dysplasia). HSIL w systemie Bethesda.
- CIN 3– neoplazja śródnabłonkowa szyjki macicy dużego stopnia (największe przemiany komórek – ang. severe dysplasia; carcinoma in situ – CIS). HSIL w systemie Bethesda.
Wirus atakuje dzielące się komórki dolnej warstwy podstawnej powodując długotrwałą i uporczywą infekcję. W wędrujących ku powierzchni naskórka (śluzówki), ulegających keratynizacji komórkach podstawnych, różnicujących się w komórki kolczyste i ziarniste dochodzi do ekspresji genów wirusa i intensywnej replikacji. Powstałe cząsteczki wirusa gromadzą się w powierzchniowych warstwach komórek, a następnie są uwalniane w złuszczonych komórkach obciążonych dojrzałymi wirusami. Ta strategia zapewnia wirusowi sukces, gdyż trwała infekcja samoodnawiających się komórek podstawnych pozwala na rozprzestrzenienie się wirusa w tkance, natomiast replikacja wirusa łączące się z ekspresją białek alarmujących układ odpornościowy gospodarza zachodzi w powierzchniowych warstwach, słabo penetrowanych przez mechanizmy obronne, co zwiększa szanse przetrwania infekcji i możliwość dalszego zakażania. Wszystkie HPV posiadają zdolność przestawienia mechanizmów komórkowych na amplifikację wirusowego DNA w zakażonych komórkach nabłonka, natomiast onkogenne HPV posiadają unikalną zdolność wprowadzania komórek dolnych warstw nabłonka w cykl podziałów komórkowych, blokując równocześnie mechanizmy kontrolne cyklu. Wiążąca się z tym niestabilność genetyczna proliferujących komórek zwiększa ryzyko nowotworzenia i jest dla gospodarza znacznie bardziej niebezpieczna niż zmiany powodowane przez wirus w ostatecznie zróżnicowanych komórkach górnych warstw nabłonka.
Brodawczak, któremu zawdzięcza nazwę rodzina HPV, jest łagodną, zwykle rosnącą na zewnątrz, zmianą wywodzącą się z zakażonego HPV nabłonka płaskiego skóry lub określonych regionów błony śluzowej. Rodzaj i wygląd zmiany zależy zarówno od typu wirusa, jak i miejsca zakażenia. Brodawki skórne stóp powodowane przez HPV 1 i 2 są silnie zakaźne i różnią się wyglądem od brodawek płaskich występujących głównie na twarzy, powodowanych przez HPV-3, 10, 26, 27 i 28.
Brodawczaki rozwijają się w wielu lokalizacjach: na skórze, wardze, w jamie ustnej, na powiece, spojówce, języku, w gardle i części ustnej gardła, w krtani i tchawicy, w przełyku, w szyjce macicy, układzie narządów płciowych i odbycie. Są zakaźne, przy czym zakaźność zależy niekiedy od lokalizacji zmiany. Brodawczaki narządów płciowych (condylomata acuminata) powodowane przez HPV 6 i 11 są niezwykle zakaźne, przenoszone w trakcie seksu waginalnego, analnego lub oralnego. Natomiast indukowane przez te same HPV 6/11 zmiany skórne w innej lokalizacji, zaraźliwe już nie są lub są mniej zaraźliwe. Typy HPV różnią się powinowactwem – tropizmem do różnych tkanek, przykładowo, brodawczak spojówki spowodowany jest zakażeniem HPV typu 6, 11, 16, 33 i 45 i nieco różni się od brodawek narządów płciowych wywołanych przez typy 2, 3, 6, 11, 16, 18 i 30-32 czy brodawczaków skórnych wywołanych przez typy 1-4 i 26-29.
dr Tomasz Ochałek
Laboratoria Medyczne DIAGNOSTYKA
Bibliografia:
- Bratosiewicz-Wąsik J. i wsp. Zakażenia wywoływane przez ludzkie papillomawirusy. Zakażenia XXI wieku: 2 , 263–271, 2019.
- McBride A. A.Oncogenic human papillomaviruses. Philos Trans R Soc Lond B Biol Sci. 2017 Oct 19; 372(1732): 20160273. Published online 2017 Sep 11.
- Fiorillo L. i wsp. Human Papilloma Virus: Current Knowledge and Focus on Oral Health. BioMed Research International, 2021. Article ID 6631757 | https://doi.org/10.1155/2021/6631757
- Mavundza E. J i wsp. A systematic review of immunogenicity, clinical efficacy and safety of human papillomavirus vaccines in people living with the human immunodeficiency virus. Hum Vaccin Immunother. Hum Vaccin Immunother. 2020;16(2):426-435. 10.1080/21645515.2019.1656481.
- Pal A., Kundu R: Human Papillomavirus E6 and E7: The Cervical Cancer Hallmarks and Targets for Therapy. Front Microbiol. Published online 2020 Jan 21. doi: 10.3389/fmicb.2019.03116.
