31/03/2020
Informacje wstępne
W związku z tym rozpoczęto dyskusję o zastosowaniu alternatywnych rozwiązań diagnostycznych. Pierwszą z propozycji jest badanie przeciwciał anty-SARS-CoV-2. Obecnie dostępne są u kilkudziesięciu producentów jakościowe testy kasetkowe, oparte o metodę immmunochromatograficzną, oceniające osobno obecność przeciwciał klasy IgM i IgG. Takie rozwiązania mogą być stosowane jako badanie laboratoryjne, ale także jako badanie POCT. W najbliższych tygodniach zostaną wprowadzone badania przeciwciał na platformy analityczne (Snibe, Abbott) i będą to badania ilościowe do użytku tylko w laboratorium.
Wszystkie oferowane rozwiązania nie mają pełnej walidacji, ze względu na skrócony czas wdrożenia w czasie epidemii (czynnik patogenny i chorobę znamy dopiero od kilku miesięcy), i są w teorii mniej wiarygodne od innych badań stosowanych w naszych laboratoriach, które przeszły pełną walidację w czasach przedepidemicznych. Dlatego też jednym z głównych wyzwań stojących obecnie przez medycyną laboratoryjną jest jak najszybsze pełne zwalidowanie dostępnych na rynku rozwiązań diagnostycznych do oznaczania przeciwciał anty-SARS-CoV-2.
Sytuacja zmienia się dynamicznie, bo codziennie pojawiają się nowe publikacje i wytyczne. Nie budzi jednak wątpliwości fakt, że badania serologiczne, wykrywające przeciwciała skierowane przeciwko wirusowi SARS-CoV-2, nie zostały zwalidowane do rozpoznawania COVID-19. Ich wyniki nie powinny być wykorzystywane jako podstawa do diagnozowania lub wykluczania zakażenia SARS-CoV-2. Takie wytyczne są pochodną faktu, że ujemny wynik badania przeciwciał nie wyklucza infekcji SARS-CoV-2. Jedynym uznanym powszechnie i zaakceptowanym badaniem do diagnozowania infekcji SARS-CoV-2 jest wykrywanie obecności wirusa w wymazie z dróg oddechowych za pomocą testów RT-PCR.
Nie znaczy to jednak, że badania przeciwciał anty-SARS-CoV-2 są bezużyteczne i nie powinny być stosowane w diagnostyce i badaniach epidemiologicznych COVID-19.
W kolejnych punktach zebrane przeze mnie dane o badaniu przeciwciał anty-SARS-Cov-2 i ich użyteczności klinicznej i epidemiologicznej.
Dane literaturowe o przeciwciałach anty-SARS-CoV-2.
Dane z poprzedniej epidemii SARS-CoV (lata 2002/2003) wykazały przydatność testów serologicznych opartych na wykrywaniu przeciwciał IgM i IgG w diagnostyce i badaniach epidemiologicznych (1,2).
Podczas obecnej epidemii wykazano, że chorzy na COVID-19 z zapaleniem płuc rozwijają równie szybką odpowiedź humoralną w klasie IgM/IgG, którą można określić przez pomiar stężenia IgM/IgG w surowicy krwi (3,4). Najdokładniejsze dane przedstawiono w publikacji Ai Tang X, Chun G, Sheng Z. Profile of Specific Antibodies to SARS-CoV-2: The First Report https://doi.org/10.1016/j.jinf.2020.03.012 skąd pochodzi poniższa rycina: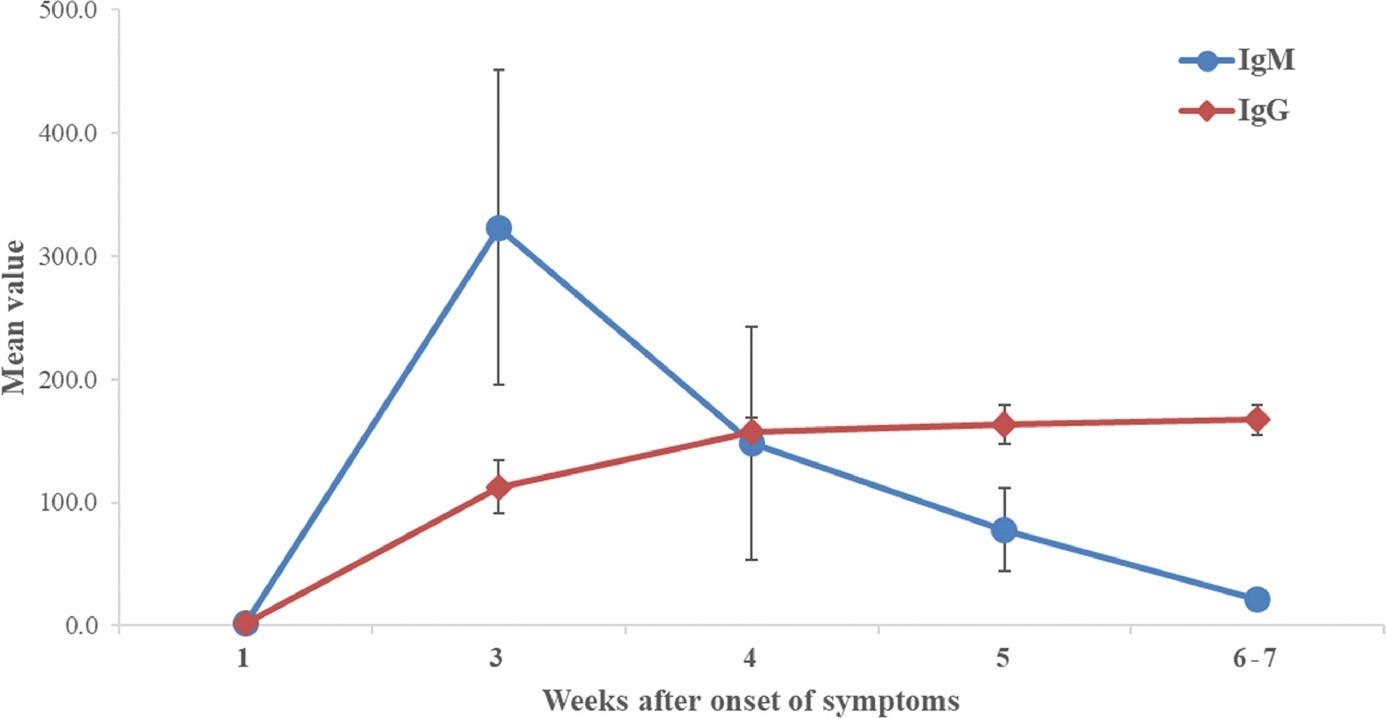
Metody serologiczne (ze szczególnym uwzględnieniem oznaczania IgM) zostały wspomniane w Zaleceniach Postępowania w Zakażeniach SARS-CoV-2 Polskiego Towarzystwa Epidemiologów i Lekarzy Chorób Zakaźnych w wersji z 24.03,2020 oraz w Laboratory Testing for Coronavirus Disease (COVID-19) in Suspected Human Cases (WHO interim guidance) z 19.03.2020, a dane z klinicznej obserwacji pacjentów hospitalizowanych w Chinach zostały podane w kilku publikacjach wymienionych na końcu tego dokumentu (3,4,5).
Po przeanalizowaniu przywołanych powyżej dokumentów można stwierdzić, że:
- Wynik badania serologicznego musi być interpretowany w odniesieniu do stanu klinicznego pacjenta, danych z wywiadu klinicznego oraz wyniku badania techniką RT-PCR wykrywającego obecność wirusa SARS-CoV-2 w drogach oddechowych.
- Dynamika odpowiedzi serologicznej w zakażeniu SARS-CoV-2 nie jest jeszcze dokładnie znana, ale najpewniej dodatnie wyniki badań serologicznych (przeciwciała w klasie IgM) pojawiają się później niż dodatnie wyniki badania RT-PCR, mniej więcej po 7-10 dniach od zakażenia.
- Wynik ujemny badania serologicznego nie świadczy o braku infekcji i nie daje podstaw do jej wykluczenia. Wynik ujemny może wystąpić u osoby zakażonej w tzw. okienku serologicznym, czyli okresie po zainfekowaniu kiedy organizm nie zdążył jeszcze wytworzyć przeciwciał odpornościowych lub w przypadkach, gdy czułość testu serologicznego jest niewystarczająca (zbyt niskie stężenie przeciwciał).
- Wyniki dodatnie badania serologicznego są najpewniej spowodowane trwającą lub przebytą infekcją wirusem SARS-CoV-2, ale mogą być także spowodowane przebytą lub trwającą infekcją szczepami koronawirusa innymi niż SARS-CoV-2, takimi jak koronawirus HKU1, NL63, OC43 lub 229E. Aby ostatecznie wykluczyć lub potwierdzić zakażenie SARS-CoV-2 należy wykonać badanie z zastosowaniem diagnostyki molekularnej techniką RT-PCR.
- Testowanie serologiczne na życzenie, obejmujące wykrywanie przeciwciał w klasie IgM, jest zasadne ze względów epidemiologicznych.
Z podanych powyżej informacji wynika, że każdy wynik badania serologicznego SARS-CoV-2 wydany przez laboratorium musi zostać opatrzony adekwatnym komentarzem, aby uniknąć błędnej interpretacji przez klinicystę lub pacjenta.
Swoiste IgM/IgG dla SARS-CoV-2 są wychwytywane w teście immunochromatograficznym przez antygen, którym jest białko nukleokapsydowe SARSr ‐ 111 CoV Rp3 (NP). Dynamika serokonwersji jest charakterystyczna dla ostrych infekcji wirusowych, tzn. początkowy wzrost IgM, a później wzrost stężenia IgG następujący wraz ze spadkiem stężenia IgM. Testy serologiczne w kierunku SARS-CoV-2 są udoskonalane przez dobór antygenu eliminującego prawdopodobieństwo reaktywność krzyżowej z innymi koronawirusami.
Jeden z producentów powołując się na publikację naukową (Okba et al., 2020, preprint) twierdzi, że testy ELISA ich produkcji, wykrywające przeciwciała w klasie IgG oraz IgA (zamiast IgM we wczesnej fazie infekcji) mają wyższą swoistość dzięki zastosowaniu jako antygenu podjednostki S1 wirusa. Podjednostka ta ma małą homologię pomiędzy koronawirusami. Reakcje krzyżowe obserwowano jedynie z SARS-CoV, a obecnie przeciwciała przeciw temu wirusowi nie są już stwierdzane w populacji. Ulotka wyklucza reakcje krzyżowe z innymi koronawirusami, ale już w artykule wykazana jest kilkuprocentowa reaktywność surowic osób zdrowych, z innymi wirusami oddechowymi, innymi koronawirusami. Producent podaje, że jego test ELISA dla klasy IgA jest czulszy, natomiast dla klasy IgG bardziej swoisty. Te dane będą podlegać weryfikacji klinicznej w najbliższych tygodniach i miesiącach.
Wybrane przesłanki dla wdrożenia serologicznych testów w kierunku SARS-CoV-2.
- Przyjmuje się, że, u osób bez niedoboru odporności, IgM staje się wykrywalna już w nawet w 3 dniu infekcji, chociaż większość cytowań podaje 7 dobę infekcji jako moment pojawienia się przeciwciał w klasie IgM, co koreluje z obniżaniem się wiremii.
- Próbki surowicy dla testów serologicznych są porównywalne, czyli niezależne od problemów technicznych związanych z pobieraniem materiału, jak to ma miejsce w przypadku materiału do badań wykrywających wirusa. Wybór materiału do wykrycia wirusa na danym etapie choroby (wymaz z gardła, popłuczyny oskrzelowe, kał) i technika pobierania wpływają na wynik. Niepoprawnie wykonanie pobranie i nie zachowanie odpowiednich warunków przedanalitycznych (czas, warunki transportu) mogą, i zapewne w pewnym odsetku przypadków, doprowadziły do uzyskania wyników fałszywie ujemnych. Natomiast w przypadku wykrywania przeciwciał w surowicy wyniki fałszywie ujemne powodowane przez problemy techniczne przy pobieraniu materiału praktycznie nie występują.
- Badaniami serologicznymi można obejmować dużą liczbę osób, poddanych do tego monitorowaniu w zdefiniowanym czasie (na przykład okresu kwarantanny). Czas do uzyskania wyniku (TAT) skraca się do godzin lub nawet minut.
- Badania serologiczne mogą być wykonywane bez względu na referencyjność placówki medycznej: w lecznictwie otwartym i zamkniętym niskiej referencyjności, w szpitalach specjalistycznych i jednoimiennych dedykowanych COVID-19.
- Prosty i szybki sposób pobierania materiału (krwi żylnej do badania) obniża narażenie na krzyżowe zakażenie pomiędzy pacjentami i narażenie personelu medycznego pobierającego materiał.
- Przeprowadzenie testu nie wymaga kosztownych, specjalistycznych laboratoriów i restrykcji zapewniających poziom odpowiedniego bezpieczeństwa biologicznego.
- Czułość diagnostyczna testów serologicznych wzrasta wraz z współistnieniem objawów typowych dla COVID-19 (np. gorączka, kaszel) i ustaleniami wywiadu (ustalenie możliwych kontaktów z zakażonymi/narażonymi itd.) zwiększającymi trafność preselekcji kandydatów do badania.
Potencjalne zastosowania badań serologicznych w diagnostyce i epidemiologii COVID-19 (szczególnie przy niepełnej dostępności badań molekularnych).
Szpitale:
- Szybki przesiew przy przyjęciu do szpitala: serologia pozytywna = wstępne potwierdzenie COVID (szybka kwalifikacja bez testu molekularnego), serologia negatywna – potrzebny wymaz i test molekularny.
- Monitorowanie pacjenta hospitalizowanego za pomocą powtarzanych badań serologicznych(7): obserwacja konwersji serologicznej, narastania i obniżania się stężenia przeciwciał.
Zastosowanie pozaszpitalne:
- Optymalizacja kwalifikacji do kwarantanny przy braku dostępności testów molekularnych. Logika: serologia pozytywna – zakwalifikowany jako chory; serologia negatywna – dalsza obserwacja/kwarantanna i możliwe powtarzanie badania.
- Monitoring epidemiologiczny pacjentów w kwarantannie i izolacji przy braku dostępności testów molekularnych. Zmiana statusu w izolacji przy dodatnim badaniu serologicznym: z obserwowany na zakażony.
- Weryfikacja monitoringu epidemiologicznego (śledzenie kontaktów pacjenta, identyfikacja “osób-rezerwuarów” wirusa, rozprzestrzenienia się infekcji w populacji, a w szczególności identyfikacja infekcji bezobjawowych).
- Szeroki monitoring populacji. Bieżące (obecnie) i retrospektywne (w najbliższych miesiącach) badania serologiczne dla celów epidemiologicznych – identyfikacja osób z przebytym zakażeniem. To zastosowanie ma najmocniejsze rekomendacje i najsilniejszy aspekt praktyczny, zarówno epidemiologiczny, jak i gospodarczy, gdyż pacjent z dodatnią serologią (i ujemnym wynikiem badania molekularnego, jeżeli jest dostępne) może wrócić do normalnej aktywności i pracy, bo przebył już infekcję i jest prawdopodobnie odporny na ponowne zainfekowanie i bezpieczny epidemiologicznie (nie przenosi infekcji).
Podstawowe informacje dla pacjentów.
- Jedynym badaniem służącym do potwierdzenia infekcji SARS-CoV-2 jest wykrycie materiału genetycznego wirusa w wymazie z dróg oddechowych za pomocą metody RT-PCR.
- Badanie to powinno być wykonane u jak największej liczby pacjentów, a w szczególności u:
- Osób z objawami klinicznymi sugerującymi infekcję SARS-CoV-2.
- Osób z kontaktu z potwierdzonymi przypadkami COVID-19.
- Badania serologiczne, wykrywające przeciwciała skierowane przeciwko wirusowi SARS-CoV-2, nie zostały zwalidowane do rozpoznawania COVID-19. Ich wyniki nie powinny być wykorzystywane jako podstawa do diagnozowania lub wykluczania zakażenia SARS-CoV-2. Wynik ujemny nie świadczy o braku infekcji i nie daje podstaw do jej wykluczenia. Wynik ujemny może wystąpić u osoby zakażonej w tzw. okienku serologicznym, czyli okresie po zainfekowaniu kiedy organizm nie zdążył jeszcze wytworzyć przeciwciał odpornościowych lub w przypadkach, gdy czułość testu serologicznego jest niewystarczająca (zbyt niskie stężenie przeciwciał).
- Badanie przeciwciał anty-SARS-CoV-2 może być wykorzystane w monitorowaniu pacjentów hospitalizowanych oraz jako badanie epidemiologiczne potwierdzające kontakt z wirusem w przypadku otrzymania dodatniego wyniku.
- Dynamika odpowiedzi serologicznej w zakażeniu SARS-CoV-2 nie jest jeszcze dokładnie znana, ale najpewniej dodatnie wyniki badań serologicznych (przeciwciała w klasie IgM) pojawiają się później niż dodatnie wyniki badania PCR, mniej więcej po 7-10 dniach od zakażenia.
- Wyniki dodatnie testu serologicznego są najpewniej spowodowane trwającą lub przebytą infekcją wirusem SARS-CoV-2, ale mogą być także spowodowane przebytą lub trwającą infekcją szczepami koronawirusa innymi niż SARS-CoV-2, takimi jak koronawirus HKU1, NL63, OC43 lub 229E. Aby ostatecznie wykluczyć lub potwierdzić zakażenie SARS-CoV-2 należy wykonać badanie z zastosowaniem diagnostyki molekularnej techniką RT-PCR.
- U każdego pacjenta z dodatnim wynikiem badania przeciwciał anty-SARS-CoV-2 powinno zostać wykonane badanie wymazu z dróg oddechowych w kierunku obecności wirusa SARS-CoV-2.
Dr n. med. Tomasz Anyszek
Specjalista diagnostyki laboratoryjnej
Specjalista zdrowia publicznego
Internista
e-mail: tomasz.anyszek@diag.pl
Referencje:
- Louie JK, Hacker JK, Mark J, et al. SARS and common viral infections. Emerging Infect Dis. 2004; 10 (6): 1143‐1146.
- Woo PCY, Lau SKP, Wong BHL, et al. Detection of specific antibodies to severe acute respiratory syndrome (SARS) coronavirus nucleocapsid protein for serodiagnosis of SARS coronavirus pneumonia. J Clin. Microbiol. 2004; 42 (5): 2306‐ 2309.
- Zhou P, Yang X‐L, Wang X‐G, et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 2020.
- Shu‐Yuan X, Yingjie W, Huan L. Evolving status of the 2019 novel coronavirus infection: Proposal of conventional serologic assays for disease diagnosis and infection monitoring. Journal of Medical Virology, 07 February 2020.
- Ai Tang X, Chun G, Sheng Z. Profile of Specific Antibodies to SARS-CoV-2: The First Report. https://doi.org/10.1016/j.jinf.2020.03.012
- Zalecenia Postępowania w Zakażeniach SARS-CoV-2 Polskiego Towarzystwa Epidemiologów i Lekarzy Chorób Zakaźnych, 24.03.2020.
- WHO: Laboratory testing for coronavirus disease (COVID-19) in suspected human cases (Interim guidance, 19.03.2020).
